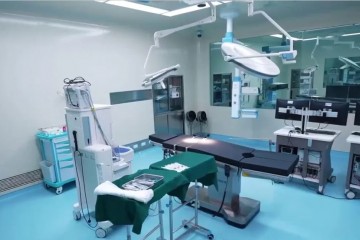
醫療器械市場規模增長強勁
2023年2月22日,羅蘭(lan) 貝格發布報告指出,2022年我國醫療器械市場規模預計達9582億(yi) 元人民幣,近7年複合增速約17.5%,已躍升成為(wei) 除美國外的全球第二大市場。中國的藥械比(醫療器械和藥品消費數據的對比)僅(jin) 為(wei) 2.9:1,遠低於(yu) 全球平均水平1.4:1和發達國家的1:1,表明我國醫療器械市場未來存在較大的增長空間。

資料來源: 弗若斯特沙利文,案頭研究,羅蘭(lan) 貝格
醫療器械上市許可持有人製度(MAH)發展曆程
- 2017年3月,國務院發布《全麵深化中國(上海)自由貿易試驗區改革開放方案》,上海自貿區內醫療器械注冊申請人可委托上海市醫療器械生產企業生產,委托生產試點;
- 2017年10月,中央辦公廳,國務院辦公廳發布《關於深化審評審批製度改革鼓勵藥品醫療器械創新的意見》,初步設立了上市許可持有人製度;
- 2017年12月,國家食品藥品監督管理總局發布《中國(上海)自由貿易試驗區內醫療器械注冊人製度試點工作實施方案》,上海自貿區開始試點;
- 2018年8月,廣東食藥監,天津市場監管委員會分別發布《關於同意開展醫療器械注冊人製度試點工作的批複》,廣東自貿區,天津自貿區開始試點;
- 2019年8月,國家藥監局發布《關於擴大醫療器械注冊人製度試點工作的通知》,試點範圍擴大到21個省市;
- 2021年6月,國務院發布《醫療器械監督管理條例》明確了醫療器械上市許可持有人製度的全麵實施。
CDMO-委托研發和生產
曆史上工程師紅利造就了國內(nei) CDMO產(chan) 業(ye) ,憑借高度專(zhuan) 業(ye) 化的研究團隊,CDMO企業(ye) 可以使新器械研發的資金投入和潛在風險在該行業(ye) 的整條產(chan) 業(ye) 鏈上得到分散,有助於(yu) 降低醫療器械企業(ye) 的研發成本及縮短研發時間,從(cong) 而加快審批及上市速度。
美敦力、強生、BD等占據市場主要份額的國外醫療器械巨頭,從(cong) 成本控製角度,都選擇逐漸剝離自身生產(chan) 負荷,轉而采用委托合同生產(chan) 模式。
可以預知的是,未來隨著醫療器械規模化上量,醫療器械領域的CDMO等服務將迎來爆發期。
哪些人是需要CDMO平台服務的?
醫生群體(ti) :
沒有專(zhuan) 業(ye) 的研發團隊;沒有產(chan) 品轉化經驗;不具備醫療器械生產(chan) 的廠房設施;不熟悉醫療器械法規;沒有注冊(ce) 和質量體(ti) 係經驗;資金不充足。
依據注冊(ce) 人製度,CDMO平台可助力醫生群體(ti) :
◆將優(you) 秀臨(lin) 床技術轉化成產(chan) 品,實現從(cong) 0到1研發,1到10的獲證;
◆推動醫療器械產(chan) 品和技術的創新;
◆加快產(chan) 品上市進程,促進優(you) 秀技術服務於(yu) 臨(lin) 床。
科研院所:
缺產(chan) 品轉化經驗;缺乏明確臨(lin) 床需求;缺產(chan) 品檢驗臨(lin) 床經驗;缺產(chan) 品上市經驗;缺乏生產(chan) 運營經驗;缺醫療器械法規解讀經驗。
依據注冊(ce) 人製度, CDMO平台可助力研發機構:
◆刺激科研積極性
◆推動醫療器械產(chan) 品和技術的創新
◆降低準入門檻
◆加快產(chan) 品上市進程
初創企業(ye) :
缺醫療器械法規解讀經驗,導致注冊(ce) 時間長;缺乏資金;建設完善的合規廠房,費耗時;創業(ye) 初期招募人員,成本高;供應鏈資源欠缺,初期采購成本高;缺乏明確臨(lin) 床需求。
依據注冊(ce) 人製度, CDMO平台可助力初創企業(ye) :
◆完善其技術、規範其體(ti) 係
◆產(chan) 品優(you) 化迭代
◆提供合規的生產(chan) 環境
◆加快產(chan) 品上市進程,盡快占領市場
那麽該如何選擇合適的CDMO公司呢?
1、看平台資源
2、看團隊和項目成果
3、看生產(chan) 能力和設施
4、看區位優(you) 勢
浙江國創醫療器械有限公司
由紹興(xing) 市越城區政府投資4500萬(wan) 元建設並持有資產(chan) ,委托國家醫療器械產(chan) 業(ye) 技術創新聯盟非營利運營(具體(ti) 簽約方為(wei) 浙江國創醫療器械有限公司),政府持有資產(chan) 聯盟非盈利運營的模式很好的解決(jue) 委托方和受托方的互信問題,並能極大的保護代工產(chan) 品的知識產(chan) 權,該平台總麵積一期即達到4000平米,涵蓋有源、無源、體(ti) 外診斷試劑等多條生產(chan) 線,可滿足不同產(chan) 品的委托需求,平台還在杭州市設立了研發部和市場部,依托聯盟及創新網團隊可為(wei) 長三角地區乃至全國提供產(chan) 品設計、代工及延伸檢驗注冊(ce) 服務。


醫療器械產(chan) 業(ye) 技術創新聯盟
◆積極響應《國家創新驅動發展戰略綱要》,科技部批複成立於(yu) 2009年6月,由業(ye) 內(nei) 創新型400+大中型企業(ye) 及科研院所組成;
◆參與(yu) 醫療器械產(chan) 業(ye) 專(zhuan) 項規劃和重點專(zhuan) 項實施;
◆搭建“產(chan) 學研醫”多方合作平台;
◆加速國產(chan) 醫療器械示範推廣應用;
◆組織國家“十二五”醫療器械重點專(zhuan) 項的啟動與(yu) 實施,總經費23.07億(yi) 元;
◆作為(wei) “十三五”“十四五”國家科技計劃項目指南編寫(xie) 及項目申請推薦單位;
服務項目
1、研發轉化:研發技術轉換、研發技術外包、研發工藝生成、樣機定型、產(chan) 品小試、產(chan) 品中試
2、生產(chan) 加工:樣品加工、OEM生產(chan) 、有源器械生產(chan) 、無源器械生產(chan) 、體(ti) 外診斷試劑生產(chan)
3、注冊(ce) 臨(lin) 床:創新申報、建立、試運行、產(chan) 品注冊(ce) 、改進、動物實驗在體(ti) 研究、臨(lin) 床備案及審批、臨(lin) 床試驗及評價(jia) 、上市後臨(lin) 床、不良反應監測。
核心服務
1、新產(chan) 品樣機研發交付和產(chan) 品迭代
2、注冊(ce) 人製度下的委托生產(chan)
3、落地當地主體(ti) ,申請許可證
核心團隊產(chan) 品經驗
1、有源,無源,IVD核心設計團隊人均15年以上醫療器械工作經驗
2、生產(chan) 團隊成員具備豐(feng) 富的上市公司生產(chan) 管理經驗
3、注冊(ce) 體(ti) 係團隊曆經數十項產(chan) 品服務經驗,細分產(chan) 品曾多次獲國內(nei) 首張注冊(ce) 證
項目成果

場地優(you) 勢
無源潔淨區、IVD潔淨區(潔淨區配套有微生物檢驗室,陰陽對照生產(chan) 區)、有源區域



區位優(you) 勢
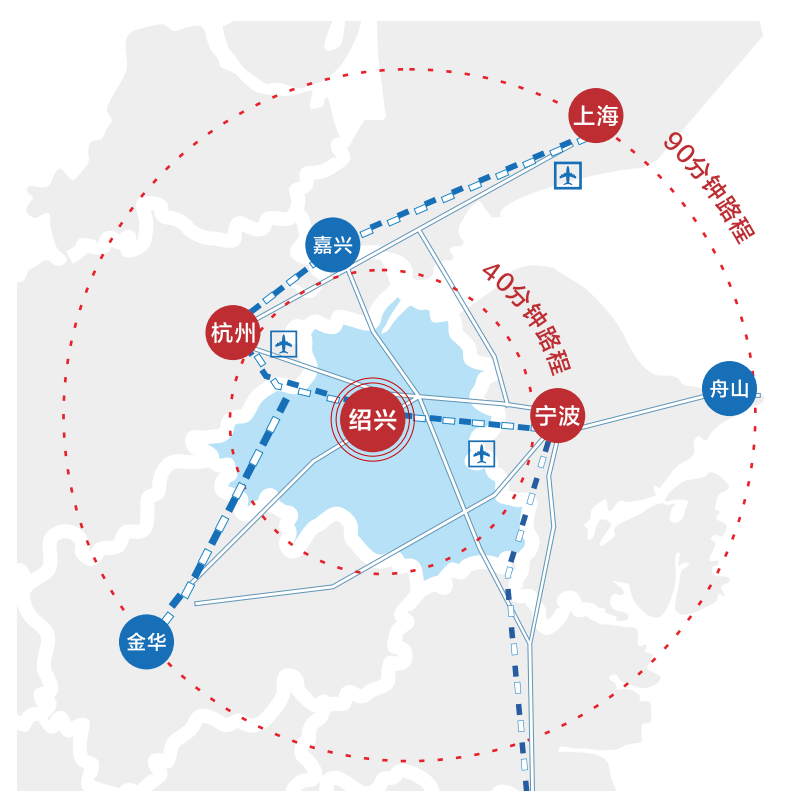
地域和空間上融入長三角一小時交通圈
核心優(you) 勢
1、醫械聯盟與(yu) 政府共同設立,非營利目的;
2、核心團隊均具備15年以上醫療器械從(cong) 業(ye) 經驗;
3、上千萬(wan) 元實驗儀(yi) 器和生產(chan) 設備;
4、4000平方米GMP廠房。